4月17日是“世界肿瘤日”,如今恶性肿瘤已超过了心脑血管疾病,成为导致居民死亡的“第一杀手”!多年来,肿瘤一直是氢氧医学研究的主要方向之一,今天为大家盘点一下氢氧医学十大肿瘤研究,看看吸氢氧这件事儿对癌症患者究竟意味着什么!
01
氢氧VS皮肤癌
1975年,《SCIENCE》论文证明,连续呼吸8个大气压的氢氧气10天(97.5%氢气,2.5%氧),高压氢氧可有效治疗动物皮肤恶性肿瘤,并认为是通过抗氧化作用。
该文首先提出氢气具有抗氧化作用的思想。但由于需要使用高压氢气,这比较复杂和危险,是许多普通生物实验室无法实现的条件,可能是没有引起太多关注的一个因素。
.png)
就像大部分初现人间的伟大事物,此文的发表像是漫漫长夜的一束星光,也没有引起太大的轰动,却默默指引着有心者向着正确的道路前行。
这篇文章中,科学家根据过去发现氢气能催化自由基反应,推测氢气会在身体内也具有这样的作用。研究对象选择癌症,是因为当时认为自由基是癌症发生的原因,氢气抗自由基也许就可以抗癌症。
遗憾的是当时研究条件有限,人们也缺乏氧气对于肿瘤作用的研究,因此实验仅能观察到氢氧吸入确实能改善皮肤癌小鼠,却无法探究真正机制,让这一发现淹没于上世纪众多科学成果之中,并没有发挥应有的价值,但其毋庸置疑仍是氢氧抗癌历程中无法忽略的,具有指引性的第一次尝试。
02
氢氧VS肺癌
肺癌,是中国及世界发病率和死亡率均居第1位的恶性肿瘤,其中80%的肺癌属于非小细胞肺癌,(非小细胞肺癌包括:鳞状细胞癌(鳞癌)、腺癌、大细胞癌)。
在“氢氧干预非小细胞肺癌”的研究中,科学家发现:吸入高浓度氢氧(66.6%氢气+33.3%氧气),可以抑制非小细胞肺癌生长,其机制与抑制Ki-67、COX-2、VEGF的表达有关···
.png)
氢氧吸入对非小细胞肺癌的抑制
科学家对瘤体组织中Ki-67、COX-2、VEGF蛋白含量进行检测,对照组有较多含量的核深染,氢氧组中这3种蛋白深染的相对较少,表明氢氧气对肿瘤有一定的抑制作用。
.png)
COX-2为环氧化酶2;VEGF为血管内皮生长因子
.png)
Ki-67是目前众所周知的一个能对细胞增殖起到标记作用的蛋白之一,其在癌组织中呈显著高表达,因此可以作为肿瘤的一个预测因子,其表达量越高,预后会越差。
COX-2的表达对于预测癌症有一定的意义,本研究通过免疫组织化学发现对照组中COX-2的含量较氢氧组显著增加,验证了氢氧作用于肺癌后具有一定的治疗意义。
肿瘤细胞的生长与血管的形成有着密切的关系,新的血管形成受机体分泌的一系列刺激因子的调节,血管的生长可以为肿瘤细胞提供连续不断的营养代谢及细胞扩增的要求,目前研究提示VEGF是作用最强的促血管形成因子,且其在恶性瘤体组织中表达量更高,经氢氧干预后,瘤体组织中VEGF的含量较对照组显著减少,表明氢氧对减少瘤体VEGF的生成有一定的积极意义。
氢氧通过抗炎症、抗氧化对抗癌症的机制已经得到证实,在患者数量最庞大的非小细胞肺癌领域,发现高浓度氢氧对Ki-67、COX-2、VEGF表达的抑制,进而说明氢氧对肺癌肿瘤的遏制作用。
以上为人类攻克肺癌的难题提供了新思路,同时高浓度氢氧抗癌再次得到有力支持。
03
氢氧VS胃癌
根据2020年全球癌症数据统计,全球范围接近一半的胃癌患者都在中国。由于饮食习惯的不同,欧美国家,每10万人中只有6、7人患胃癌,而在中国每10万人中就有30人患胃癌。
为了研究氢氧对胃癌的作用,国内顶尖医研机构——复旦大学中山医院的科学家进行了一项氢氧混合吸入抑制胃癌细胞增殖和迁移的实验,并在2021年将实验成果发表在国际期刊《Cancer Cell International》上。
在该实验中,科学家购买人类胃癌细胞“MGC-803”、“BGC-823”,并在改良的培养基中进行培养。然后将这些胃癌细胞分为氢氧组和对照组。
科学家首先研究了氢氧气是否会影响胃癌细胞的增殖。在氢氧混合气体暴露24小时后,与正常培养的MGC-803和BGC-823细胞相比,存活的MGC-803和BGC-823细胞减少了20%以上。
.png)
此外,氢氧混合气体(66.6%氢气+33.3%氧气)使MGC-803细胞的运动能力显著降低约60%,使BGC-823细胞的运动能力显著降低50%以上。
科学家还发现,氢氧可以显著抑制胃癌细胞MGC-823中lncRNA MALAT1(促癌)和转录因子EZH2(促癌)的表达,同时上调miR-124-3p(抑制前两者)表达,三者关系如下:
IncRNA MALAT1已经被证明可促进癌细胞的增殖和迁移
EZH2的突变或者过表达与多种类型癌症相关,如乳腺癌、前列腺癌、黑色素瘤和膀胱癌等。因为异常激活的EZH2可以抑制“抑癌基因”的正常表达,所以抑制EZH2的活性可以使肿瘤生长变慢。
miR-124-3p被鉴定为IncRNA MALAT1的靶点和调节因子。同时,EZH2的表达也被miR-124抑制。
而氢氧可以上调miR-124,氢氧环境下,EZH2和lncRNAMALAT1的表达都被抑制,所以胃癌细胞被抑制。
.png)
胃癌细胞对照组(CK)和氢氧组(H2)基因组表达对比,抑制最明显的前两个基因分别是lncRNAMALAT1和EZH2。
以上表明,如需一步研究氢氧VS胃癌,lncRNA MALAT1/miR-124-3p/EZH2轴可能是一个新的干预靶点。该实验证明了人类胃癌细胞被氢氧抑制,该结果为未来氢氧对抗人类胃癌的临床应用打下基础。
04
氢氧VS卵巢癌
卵巢癌常常被看作是女性肿瘤的“隐身杀手”,由于卵巢位于盆腔深处,位置隐秘,初起症状轻微,常规妇科检查一般只能查到卵巢囊肿。
为了研究氢氧对卵巢癌的作用,研究者首先建立了卵巢癌的模型:选取两种卵巢癌细胞Hs38.T和PA-1皮下接种到实验小鼠上,两周后即可观察到肿瘤的生长。然后将之随机分为两组:其中一组是氢氧组,该组小鼠每天吸氢氧三次(66.6%氢气+33.3%氧气)每次30分钟,连续吸氢氧6周;另外一组为对照组,呼吸正常空气。
两组小鼠除呼吸不同外,其余均在相同条件下进行饲养。实验结果如图所示,6周氢气吸入能显著抑制肿瘤生长,肿瘤体积平均缩小32.3%,其中一项表征肿瘤恶性增殖程度的指标Ki67表达下降30%,这说明肿瘤生长得到了显著的抑制。
.png)
在氢氧环境中,卵巢癌细胞的侵袭能力和迁移能力均显著下降,这提示氢氧可能会抑制卵巢癌细胞的转移。要知道,肿瘤的复发转移才是导致患者死亡的主要原因,如何抑制肿瘤复发转移一直是肿瘤治疗的最大难题。
05
氢氧VS鼻咽癌
鼻咽癌是头颈部最常见的恶性肿瘤之一,全世界约一半以上病例见于中国,多见于中国南方和东南沿海地区。鼻咽癌主要采用单纯放疗或放化疗结合。由于包括中耳、耳蜗、听觉神经、脑干和听觉皮层在内的整个听觉系统都位于或靠近用于鼻咽癌治疗的照射区域,因此来自放射治疗的辐射不可避免地涉及这些结构。
放射治疗后通常会出现分泌性中耳炎、听骨链坏死和耳蜗及听神经损伤等并发症。听力损伤是鼻咽癌放疗后最常见的晚期不良反应。随着患者存活时间的延长,这种并发症变得越来越严重,严重影响了患者的生活质量。到目前为止,还没有特殊的治疗方法,使得鼻咽癌康复非常困难。
去年,《Frontiers in Medicine》发表重要研究成果,首次前瞻性研究报道氢氧吸入(66.6%氢气+33.3%氧气)对长期生存的鼻咽癌放疗/放化疗后耳聋患者的听力具有改善:随着吸氢氧时间的增加,患者听力呈现进一步改善的趋势,且安全性好,长期吸入氢氧气体可能是这类鼻咽癌患者可选择的康复疗法。
.png)
发表在《frontiers in Medicine》上的文章
入选临床研究的患者均符合以下条件:
(1)经病理检查确诊为I期至IVb期鼻咽癌;
(2)5年前接受过常规放疗(放疗)或放疗联合化疗(化放疗);
(3)抗肿瘤治疗前听力及听力检查结果正常;
(4)在60岁或更低年龄时经历听力损失,这排除了老年性耳聋的可能性;
(5)吸入氢氧至少4周。
患者的中位年龄为58周岁,这与中国鼻咽癌放化疗患者群体基本符合。
听力损失发生在放疗或化放疗结束后24至289个月,中位时间为117个月。患者治疗前的平均气导、骨导听力分别为77.46±28.12dB、46.76±20.73dB,大部分患者已达中重度听力损害水平,且均存在逐年加重的情况。
结果显示,单纯放疗者、放化疗患者,气导及骨导听力阈值均有显著提高。这表示,氢氧吸入对放化疗患者改善更明显,提示氢氧对于化疗所致的听力损害也有改善作用。
.png)
(上排三图为放疗,下排三图为放化疗)
放射治疗过程中,活性氧(ROS),尤其是羟基自由基(OH−)和过氧亚硝基胺大量产生;氧化应激促发炎症反应。在放射性损伤的进展中细胞凋亡及血管损伤和内皮功能障碍起重要作用。
目前的研究表明氢氧具有抗氧化抗炎症作用,可以对抗放疗引起的氧化应激和炎症。其次,氢氧具有细胞保护活性,可以改善放疗诱发的细胞凋亡。最后,氢氧有改善血液灌注的作用,可以减轻放疗导致的血管性损伤。
06
氢氧VS胆囊癌
这是一篇发表在《World J Clin Cases》上的个案报道,一名72岁女性患者 ,表现为转移性胆囊癌,对症治疗联合氢氧吸入。(66.6%氢气+33.3%氧气)
在开始吸氢氧后,患者的躁动减少,两周后完全消失,患者睡眠时间从4个小时每天延长到8~10个小时每天。
患者吸氢氧后,血清ALT、AST、TB和GGT水平均未出现异常,红细胞计数和血红蛋白水平停止下降,输血间隔时间从1周延长到2周,红细胞计数和血红蛋白吸氢氧一个月后开始升高,如下图:
.png)
同时血清总蛋白、白蛋白水平也开始升高,如下图:
.png)
入院时,血清CA19、AFP、CEA均升高,吸氢氧后,三项指标未立刻下降,但两个半月后,三项指标迅速下降恢复正常!
.png)
分析CT值,患者吸氢氧后,肿瘤多发直径之和也从12.2cm到16.7cm,最后降低到8.1cm!CT图如下:
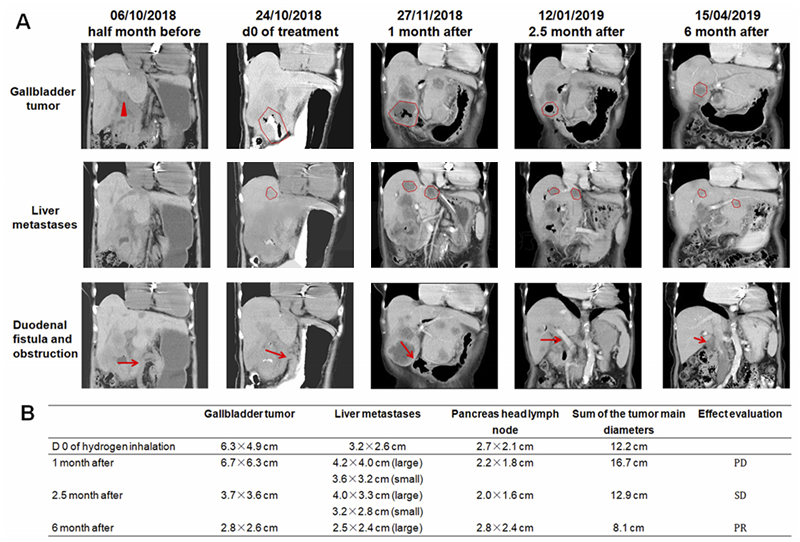
该实验虽然是个案,但价值在于通过实践证明——尽管胆囊癌治疗困难,但氢氧依然能起到作用。
本例患者在诊断时存在肝内和肝门静脉转移,侵犯十二指肠并出现胰腺头部周威,多次淋巴结转移累及下腔静脉提示转移性癌,而且患者72岁无法接受常规抗癌治疗。吸氢氧1个月后,血液指数改善,两个半月后十二指肠梗阻逐渐消失,胃管拔除,肿瘤标志物下降,CT检查显示肿瘤逐渐减少。
07
氢氧VS肝癌预防
肝癌是我国发病率第四位、死亡率第三位的恶性肿瘤,中国新发肝癌占全球55%,五年生存率仅10%左右,这是恶性肿瘤中预后最差之一,因此,肝癌也被称作“癌症之王”。
肝癌为何难治?因为肝癌具有“异质性”的特点,所谓“异质性”指的是临床上,处于同一分期,临床病理特征相似的肝癌患者,手术切除后的复发转移率和生存率,以及对药物治疗的反应,往往显著不同。肝癌的异质性具有普遍性和多层次,因此肝癌的治疗往往也是最为复杂的,所以肝癌治疗难度更大。
目前氢氧医学领域已开始对肝癌进行研究,也有部分案例被报道。在氢氧预防肝癌的的研究中,最重要的一篇当属山东两家医学机构携手发布的氢氧抑制脂肪肝的临床研究。(中国有近3亿人口患有脂肪肝,而脂肪肝炎又是引发肝癌的重要因素,因此改善脂肪肝,也可视作对肝癌的控制和预防。)
本次实验经山东泰山医学院伦理委员会批准,在所有患者签署知情通知书的情况下,筛选62位非酒精性脂肪肝(NAFLD)患者参与本次实验。这些受试者被随机分入2个组,一组32人,为安慰剂组,吸入主要为78.1%氮气+20.9%氧气的混合气体,第二组30人,为氢氧组,吸入66.6%氢气+33.3%氧气的高浓度氢氧混合气体。
两组吸入均持续13周的时间。最终安慰剂组21人坚持完成该临床研究,氢氧混合吸入组22人坚持完成。
受试者情况汇总

研究团队评价了受试者脂肪肝严重程度,氢氧吸入组试验前/后,轻度、中度、重度数据如下:
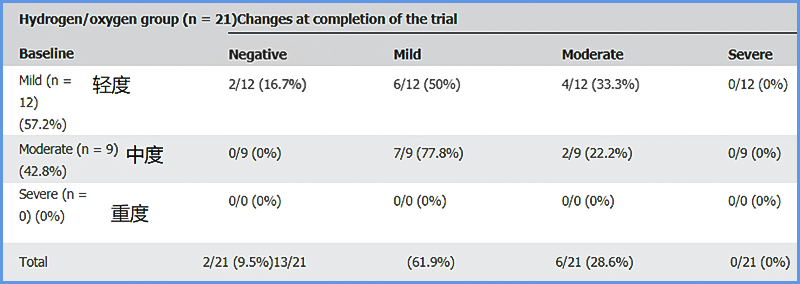
安慰剂组试验前/后,轻度、中度、重度数据如下:
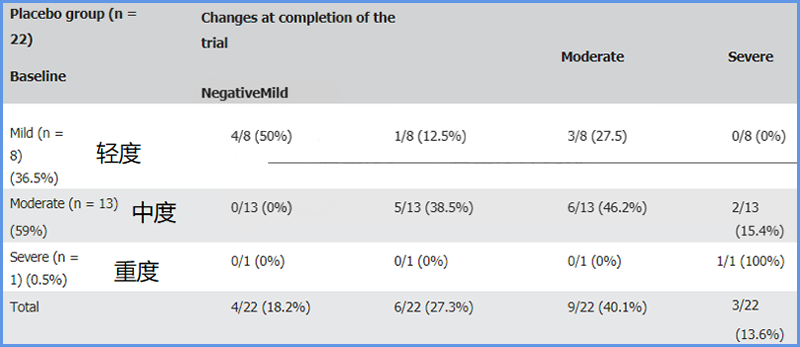
从上述两个表的数据可以看出,受试者中,氢氧吸入组改善为轻度的比例更多,氢氧吸入后没有重度脂肪肝出现。
该实验中,研究者还对比了两组的CTL/S(肝脾CT比例,其中肝英文为Liver,脾英文为Spleen,CT是密度值,CTL/S表示肝和脾密度比,脂肪肝患者,肝脏脂肪含量高,脂肪密度小,则CTL/S越小,脂肪肝越严重,其中,CTL/S<0.838表示至少有30%脂肪肝变性,越小越严重!)
以下是两组CTL/S的指标对比:
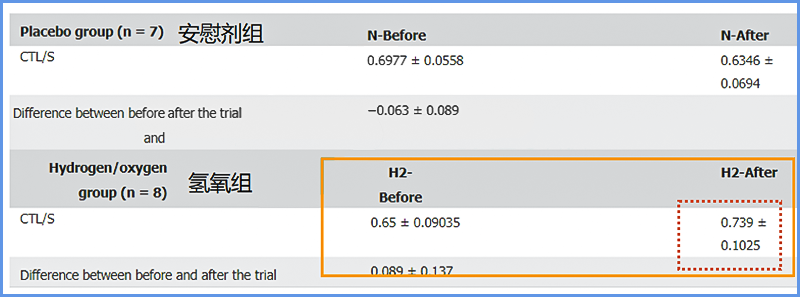
上图可以看出,安慰剂组试验前后、以及氢氧组试验前CTL/S的数据都差不多,只有氢氧组试验后出现明显改善,数据从0.6级增加到0.7以上,这说明脂肪肝因为吸入氢氧气改善明显。
这个实验不仅对于肥胖人士减肥具有重大价值,同时氢氧也作为一种尚未发现毒副作用的气体,通过改善脂肪肝达到长期保护肝部,预防肝癌的可能性被成功验证。
08
氢氧VS肿瘤生长
在全球第一部氢氧吸入抗癌专著《氢气抗癌:理论和实践》中,研究者通过动物试验揭示了氢氧吸入(66.6%氢气+33.3%氧气)对肿瘤细胞生长的抑制情况。
在该实验中,研究者将动物(小鼠)分为2组:正常组和氢氧组。研究者给实验动物注射肿瘤细胞成瘤,分别观察正常组和氢氧组体内肿瘤生长情况,并统计对比。结果发现:随着时间的推移,正常组体内肿瘤生长速度由慢到快,氢氧组体内肿瘤保持慢速增长,结果如下:

正常组和氢氧组肿瘤生长曲线对比
干预方法:正常组注射肿瘤后不做处理,在正常环境下饲养;氢氧组同样在正常环境下饲养,另外每天给予6小时氢氧混合吸入,流量为3L/min,共14天。结果显示,正常组肿瘤生长速度明显快于氢氧组。
研究者最终将两组小鼠解剖查看肿块大小,结果氢氧组的肿瘤明显小于正常组,照片如下:
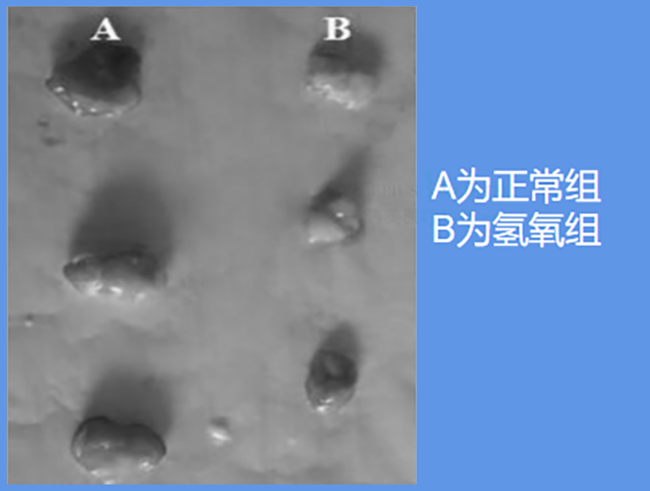
这次试验尽管不是人体临床,但很直观地观察到高浓度氢氧混合吸入对肿瘤的抑制。高浓高度氢氧混合气(66.6%氢气+33.3%氧气)在充分氢气的基础上兼顾氧气吸入,避免缺氧微环境,这原本是从过往临床案例得出的方向。未曾设想的是,2021年《Natrue》子刊的一篇重磅论文解释了氧气对于抗癌的价值。
该文章发现,缺氧微环境下,更适合肿瘤细胞转移生长。因此氢氧吸入在抗癌中发挥了双作用。这次动物实验的结果也为后续氢氧抗癌研究找到了正确方向。
09
氢氧VS肿瘤细胞增殖
上述研究团队发现氢氧对动物肿瘤生长的抑制作用以后,通过细胞培养的方法,直观观察氢氧气体对肿瘤细胞的影响。
研究者将A549细胞(肺癌人类肺泡基底上皮细胞)分为正常组和氢氧组(66.6%氢气+33.3%氧气)进行体外培养,每隔两天更换一次营养液,长满后进行传代,传代的A549细胞继续按照亲代的环境培养,持续观察2组细胞到第10代。
结果发现:第一代,2组没有明显差异,增殖情况类似,细胞状态较好;第五代时,氢氧组A549细胞增殖受到明显抑制,肿瘤细胞的体积增大、死亡比例增多;第十代时,氢氧组出现很多空泡化的细胞。

显微镜下,可以看到氢氧组的肿瘤细胞传代后逐渐死亡、减少。
这次试验成功观察到氢氧气如如何促进肿瘤细胞的凋亡,如何抑制肿瘤增殖和生长。
10
氢氧改善免疫
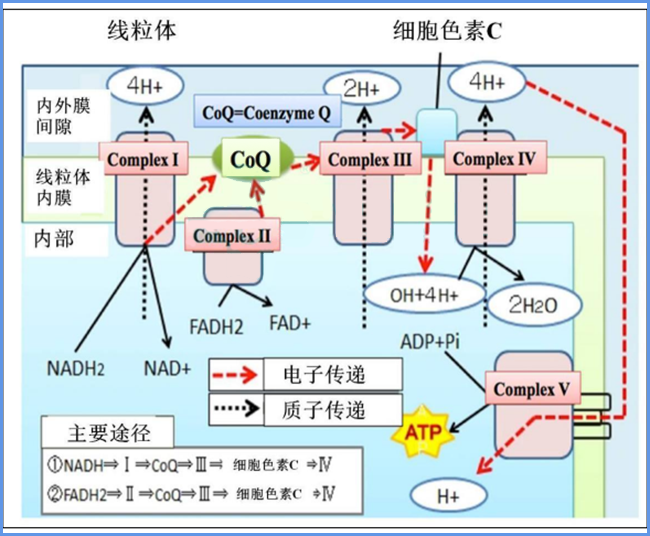
辅酶(Co)Q10是线粒体呼吸链中必不可少的电子载体,如下图所示,将复合物I和II中的电子传递到复合物III中,催化•OH与分子氢结合形成水分子,进而消灭•OH。因此,我们认为外周血CoQ10浓度可以看做是线粒体功能的一个有用的标志物,与线粒体功能呈正相关。
在氢氧激活线粒体免疫的实验中,科学家发现,氢氧吸入导致癌症患者外周血中PD-1+(耗竭性)CD8+T细胞的比例降低和PD-1−(非耗竭性)CD8+T细胞的比例升高。
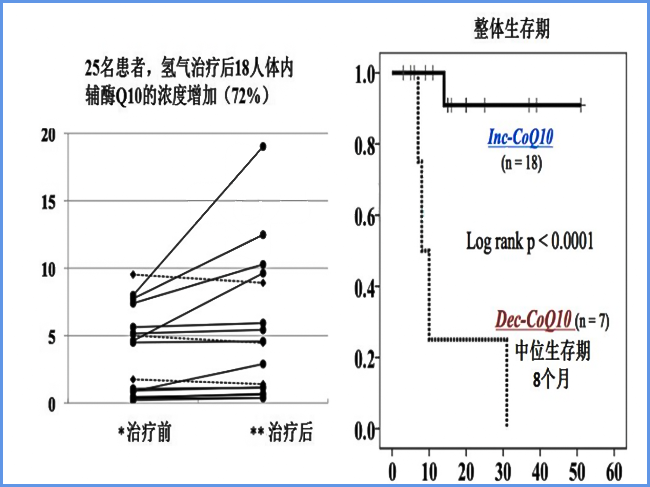
挑取25名肿瘤患者,检测了血液中CoQ10的表达情况,发现在氢氧吸入后有18例(72%)患者CoQ10浓度升高。与CoQ10降低的患者(中位OS=8个月)相比,CoQ10升高的患者总体生存率(> 50 个月)显著提高,表明氢氧可能通过增加CoQ10的含量来改善T淋巴细胞的线粒体功能,进而提高患者存活率,如下图:
该实验首次发现了吸氢延长肿瘤患者生存时间的免疫学证据,是升高血液中的高活性(PD-1—)T细胞数量,降低耗竭性(PD-1+)T细胞比例,延长杀伤性T细胞的生存时间和杀伤能力,进而显著延长患者PFS和OS。实现这一效果的机制,可能是升高T淋巴细胞线粒体内膜上的CoQ10表达水平,使更多分子氢能够进入线粒体内部,中和•OH来保护线粒体的正常功能。
结语
过去大量研究表明,肿瘤的发生和炎症、氧化应激紧密相关,而氢氧吸入就是人类对抗炎症、氧化应激最有效的法宝之一,氢氧对多种不同类型的肿瘤均表现出抑制作用,上面十个研究仅仅是氢氧控癌的冰山一角。
氢氧除了预防、对抗肿瘤以外,在肿瘤放化疗副作用的改善上也有大量科学实践,其中就包括发表在《Medical Gas Research》上的““Real world survey” of hydrogen-controlled cancer: a follow-up report of 82 advanced cancer patients”,结果显示氢氧吸入对患者放化疗副作用的减轻,对于患者自理能力、生活品质的提升···这些研究对于人类未来依靠氢氧战胜癌症贡献了宝贵参照。